肠道菌群对于健康的重要性一直被强调,前有报道可以通过改变肠道菌群养成 “瘦子体质”,后有通过肠道菌群改善脂肪肝及多器官健康的报道,可见,“万能的肠道菌群”已经在多方面得到证实。那么肠道菌群与阿尔兹海默症之间是否也存在某些关联呢?
最近,一篇发表在Brain的题为Microbiota from Alzheimer’s patients induce deficits in cognition and hippocampal neurogenesis的文章,首次证实了肠道微生物群在阿尔茨海默病中的因果作用,阿尔茨海默氏症的症状可以通过肠道微生物群转移到健康的年轻生物体上。
该研究招募了阿尔茨海默病(AD)患者 ( n = 69)和认知健康对照者( n = 64),将他们粪便中的微生物移植到大鼠中。大鼠在使用抗生素7天后,随机分为两组,接受来自对照组和AD组的肠道微生物。之后收集粪便进行16S微生物组学和生物信息学分析,并进行行为学测试等。
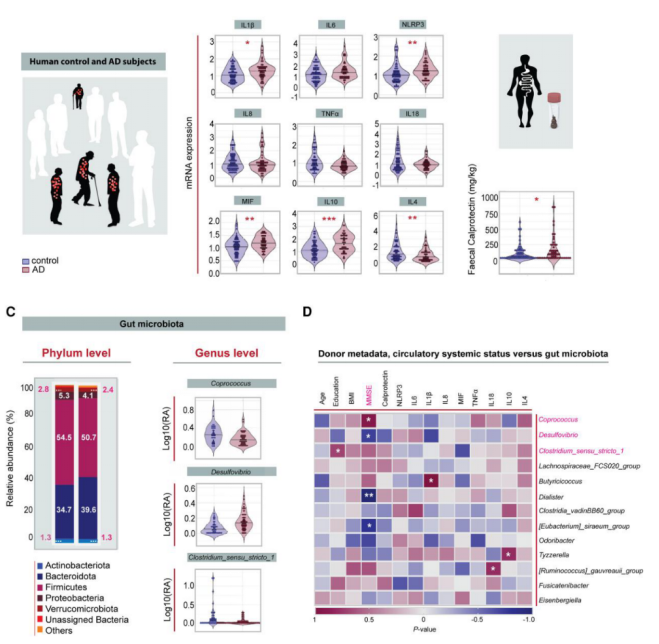
首先,该研究对69名健康对照者和64名AD病患者的血浆及肠道菌群进行评估,发现AD患者全身炎症增加,并且在AD患者肠道中,与促炎相关的微生物丰度增加,而产生有益代谢物微生物较少。为了进一步了解这些变化是否与AD患者的临床状态相关,将简易精神状态评分(MMSE)与肠道菌群的变化相关联,发现MMSE与肠道菌群特征之间存在显著的相关性,也就是说阿尔兹海默症与肠道菌群之间存在因果关系。
https://doi.org/10.1093/brain/awad303
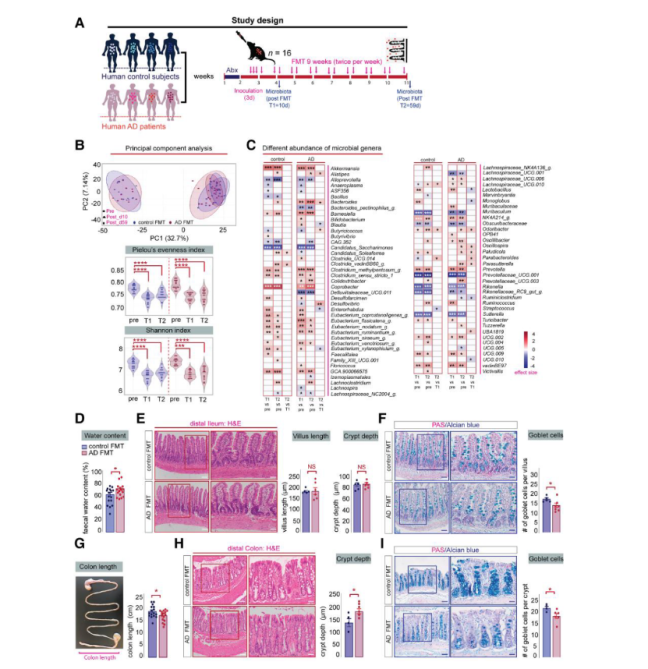
为了探究这种因果关系,研究者将健康者和AD患者的粪便样本移植到成年大鼠体内,移植前通过抗生素处理去除大鼠肠道原有的微生物。在移植后的10天和59天对粪便和肠道健康等进行了分析。平均40 %分类单位的微生物植入受体大鼠,78个菌属在受体大鼠中发生了显著变化。与原始微生物群相比,植入AD患者粪便的大鼠显示出比大对照组大鼠更显著的微生物属的变化,并且差异较大的菌属与MMSE评分有关。为了进一步阐明AD肠道微生物群是否诱导健康老鼠胃肠道的病理生理过程,研究者评估了粪菌移植后大鼠肠道的健康状况。结果表明,植入对照组的微生物后,大鼠结肠组织中促炎细胞因子基因表达无明显差异,未发生胃肠道局部炎症事件。而植入AD患者微生物的大鼠表现出粪便含水量和摄入量的显著增加以及结肠长度的减少、结肠粘膜损伤等症状,表明AD患者肠道微生物群对结肠功能的特定影响。
https://doi.org/10.1093/brain/awad303
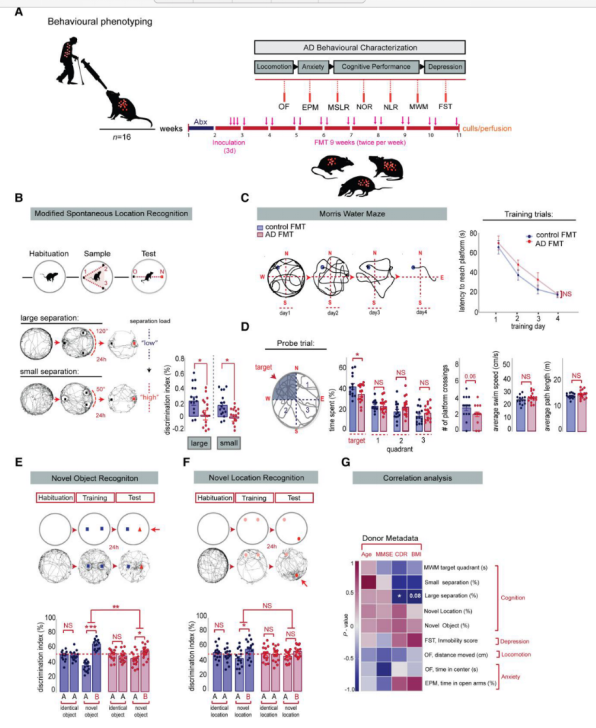
为了研究肠道微生物群与AD症状的关联,研究人员进一步评估了粪菌移植后大鼠的行为学表现,以评估记忆表现和其他阿尔茨海默病相关并发症。结果发现,植入AD菌群的大鼠对熟悉和新奇位置的辨别能力显著受损,在其他记忆表现任务中也得到相似结果,并且表现出长期空间记忆受损。总的来说,来自AD患者的肠道微生物群的存在促进了与AD临床症状相关的认知缺陷,并损害了受体大鼠成人海马神经发生(AHN)依赖的记忆表现。
https://doi.org/10.1093/brain/awad303
进一步通过检测新生神经元的存活情况,发现与对照组受体大鼠相比,AD组受体大鼠新生神经元的存活减少,而这些新神经元已被证明有助于记忆的能力。为了深入了解可能导致阿尔茨海默病定植大鼠记忆缺陷的机制,研究者进一步使用细胞进行了3D重建,以评估其树突的复杂性。发现与对照组受体大鼠相比,观察到AD定植大鼠的树突复杂性显著降低。数据表明,从AD中转移的肠道微生物群负向影响成年出生的神经元的存活和树突分支。
另外,该研究通过体外神经发生实验来研究AD的系统环境如何调节海马神经发生。将人胚胎海马祖细胞(HPCs)暴露于对照受试者和阿尔茨海默病患者的血清中,并测定了表达神经干细胞增殖、分化和程序性细胞死亡标志物的细胞百分比。结果表明,阿尔茨海默病患者血清降低了HPCs的增殖分化能力并且损害神经元分化。值得注意的是,将这些观察结果与阿尔茨海默病患者的临床表型联系起来。发现特定细菌属与神经发生标志物相关联,也与MMSE评分高度相关,表明神经发生受损可能是肠道微生物群组成改变与阿尔茨海默病认知障碍之间的联系。
最后,为了更好地了解是哪些因素可能触发AD患者肠道菌群转移对记忆和相关行为的影响,进一步将对照组和AD定植大鼠的盲肠内容物和海马组织进行了非靶向代谢组学分析。结果显示,盲肠内容物的13个代谢物和海马组织中的3个代谢物,在AD患者植入大鼠与对照定植的大鼠差异显著。包括组氨酸、色氨酸代谢物等代谢物的增加,这些都与AD症状发生有关。
总的来说,该研究发现揭示了阿尔茨海默病的症状可以通过肠道微生物群转移到健康的年轻生物体中,证实了肠道微生物群在阿尔茨海默病中的因果作用。科学家们正在努力制定策略,通过探索肠道微生物群如何对饮食和运动等生活方式的影响做出反应,促进健康的大脑衰老和推进阿尔茨海默氏症的治疗。
参考文献:https://doi.org/10.1093/brain/awad303
来自: 生物谷
更多阅读: