说起危害心血管健康的“坏胆固醇”,很多人都会想到低密度脂蛋白胆固醇(LDL-C)。实际上,脂蛋白(a)是比LDL-C更“恶毒”的存在。
越来越多的证据表明,与LDL-C类似但粘性更强的脂蛋白(a), 是动脉粥样硬化和主动脉瓣狭窄的致病因素,其水平降低与心血管事件减少独立相关[1]。目前市场上尚无批准的治疗方法,而且很难通过改变生活方式来改善[2]。
今日,首个用于降低脂蛋白(a)的小分子药物Muvalaplin, I期临床试验结果在JAMA期刊上公布,并同步于近期召开的欧洲心脏病学会年会(2023 ESC)。
澳大利亚蒙纳士大学维多利亚心脏研究所的Stephen J. Nicholls教授带领其团队完成这项I期临床研究。114名参与者的数据表明,持续14天每日口服Muvalaplin可将血液中脂蛋白(a)水平最多降低65%,无显著的不良反应[3]。
论文首页截图
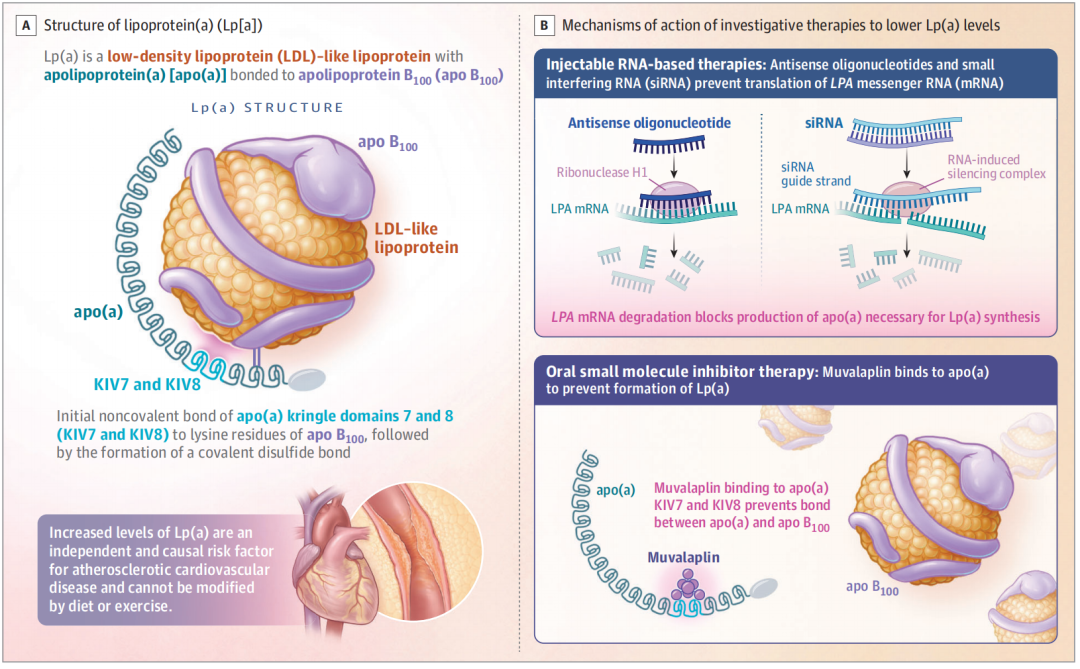
肝脏中合成的载脂蛋白(a) (apo[a]),与低密度脂蛋白样颗粒上的apo B100蛋白,通过非共价结合形成脂蛋白(a)。
当前,已开发有反义寡核苷酸(ASO)[4]、小干扰RNA(siRNA)药物[2,5],通过减少肝脏合成apo(a)来降低脂蛋白(a)水平,这些药物目前处于不同的临床阶段。
值得关注的是,靶向脂蛋白(a)的siRNA药物Olpasiran的II期临床数据突出,于去年11月公布在《新英格兰医学杂志》期刊上,显示可将脂蛋白(a)水平降低高达96%。其最新数据同样于近期在欧洲心脏病学会年会上公布,提示在最后一次给药近一年后,脂蛋白(a)水平持续降低。
不过,这些药物都属于注射疗法。
Muvalaplin是一种小分子口服药物,通过阻断 apo(a)-apo B100相互作用来抑制脂蛋白(a)形成。Stephen J. Nicholls团队在这项I期临床试验中,完成对Muvalaplin的安全性、耐药性、药代动力学等评估。
脂蛋白(a)以及当前临床药物的主要研发方向
研究共纳入114名年龄在18-69岁、体质指数≤30的参与者,分为两组,分别为只接受单次给药的单次剂量递增组(n=55),和持续14天每日给药的多次剂量递增组(n=59)。每组中有不同比例的参与者接受安慰剂或Muvalaplin治疗。
单次剂量递增组和多次剂量递增组参与者的平均年龄为29岁、32岁,女性占比为64%、58%,基线中位脂蛋白(a)水平为 10.3mg/dL和58.3mg/dL,基线中位LDL-C水平为104.4mg/dL和116.0mg/dL。
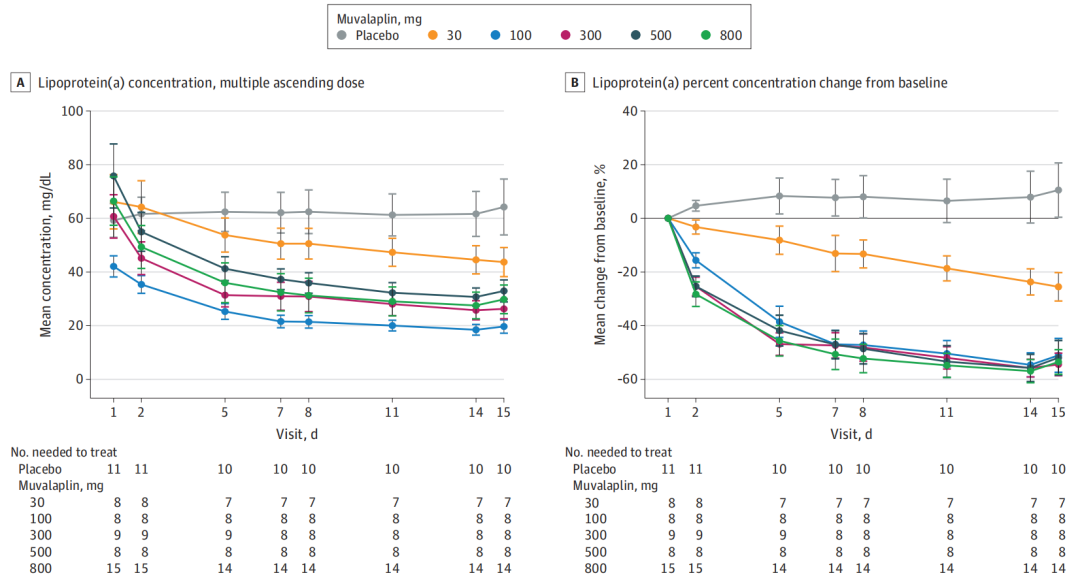
结果显示,连续14天口服30-800mg剂量,会导致Muvalaplin血浆浓度增加,半衰期为70-414小时。首次给药后24小时内,Muvalaplin可降低脂蛋白(a)的血浆水平,重复给药后进一步降低,且呈剂量依赖性降低。
14天治疗结束时,与安慰剂治疗相比,每日服用剂量≥100mg可以使参与者脂蛋白(a)水平下降63%-65%,有93%的参与者脂蛋白(a)水平低于50mg/dL。每日口服剂量为300-800mg时,参与者脂蛋白(a) 水平在数十天内持续下降,距离最后一次Muvalaplin给药后64天升至基线水平。
每日服用Muvalaplin对血浆中总胆固醇、LDL-C、高密度脂蛋白胆固醇、甘油三酯和apo B100水平没有影响。
Muvalaplin口服治疗降低脂蛋白(a)的效果
治疗相关的不良事件大多是轻度的、短暂的,并在无后遗症的情况下得到缓解。没有发生剂量依赖性的不良事件,无死亡或严重不良事件。每日口服Muvalaplin的参与者中,头痛(20%)、腹泻(15%)、腹痛(10%)等最为常见。
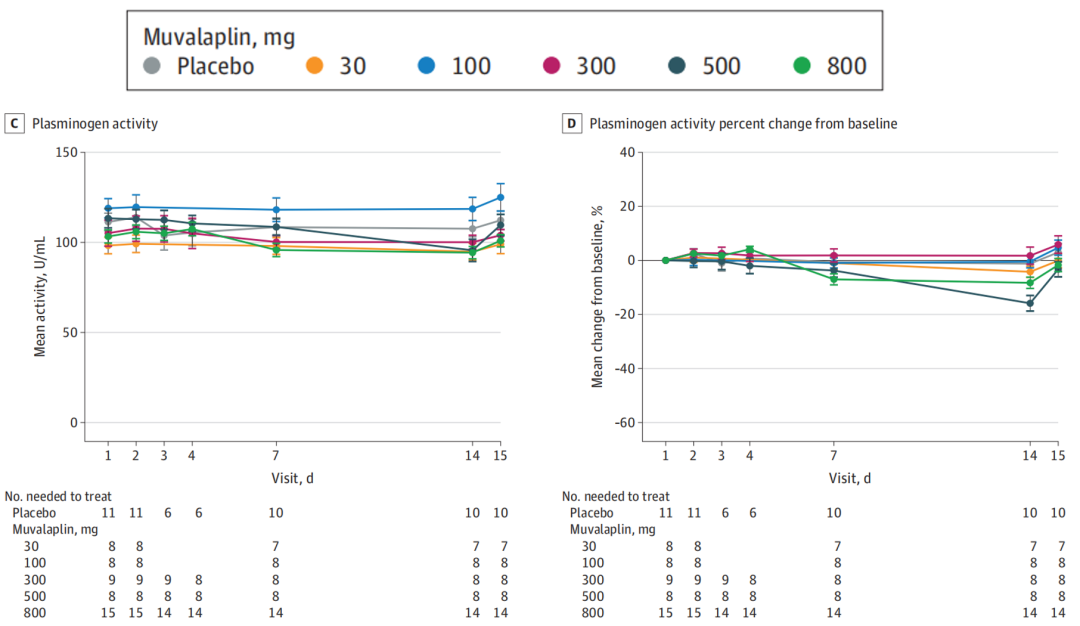
另外,由于脂蛋白(a)的组成部分apo(a),与纤溶酶原之间具有密切的同源性,因此理论上通过Muvalaplin降低脂蛋白(a)可能会影响止血和凝血功能。
检测结果显示,止血功能指标以及纤溶酶原活性在高剂量下有轻微变化(500mg剂量时最多降低约14%),但在停药后恢复到基线。
血液中高敏C-反应蛋白水平未显示显著变化。
纤溶酶原活性在治疗期间的变化
总体来说,这项I期临床试验表明,口服Muvalaplin能够有效较低脂蛋白(a)水平,且没有严重副作用。接下来,还需要更长时间、更大规模的试验来进一步评估 Muvalaplin的安全性、耐受性,以及对脂蛋白(a)水平和心血管疾病结局的影响。
参考文献:
[1]Bittner VA, Szarek M, Aylward PE, et al; ODYSSEY OUTCOMES Committees and Investigators. Effect of alirocumab on lipoprotein(a) and cardiovascular risk after acute coronary syndrome. J Am Coll Cardiol. 2020;75(2):133-144. doi:10.1016/j.jacc.2019.10.057
[2]O’Donoghue ML, Rosenson RS, Gencer B, et al; OCEAN(a)-DOSE Trial Investigators. Small interfering RNA to reduce lipoprotein(a) in cardiovascular disease. N Engl J Med. 2022;387(20):1855-1864. doi:10.1056/NEJMoa2211023
[3]https://jamanetwork.com/journals/jama/fullarticle/2808864
[4]Tsimikas S, Karwatowska-Prokopczuk E, Gouni-Berthold I, et al; AKCEA-APO(a)-LRx Study Investigators. Lipoprotein(a) reduction in persons with cardiovascular disease. N Engl J Med. 2020;382(3):244-255. doi:10.1056/NEJMoa1905239PubMedGoogle ScholarCrossref
[5]Nissen SE, Wolski K, Balog C, et al. Single ascending dose study of a short interfering RNA targeting lipoprotein(a) production in individuals with elevated plasma lipoprotein(a) levels. JAMA. 2022;327(17):1679-1687. doi:10.1001/jama.2022.5050
来自: 奇点网
更多阅读: