运动的好处,实在是数也数不完。
运动能够对抗各种年龄相关疾病的代谢和免疫变化,降低心血管疾病和癌症的死亡风险;对于患有2型糖尿病或血脂异常的人来说,运动能够显著改善生理指标;运动与帕金森病、阿尔茨海默病等神经退行性疾病风险较低有关;近期还有研究发现,运动能够重塑衰老的免疫系统,这能降低对多种疾病的易感性。
近期,发表在《细胞·干细胞》杂志上的一项研究[1]更为细致地分析了运动给多种干细胞带来的好处。通过对43万余个细胞的单细胞转录组分析,研究者发现,运动能够改善衰老带来的多种炎症通路上调、恢复胞间通讯、增加骨骼肌中的蛋白表达并改善肌肉再生。

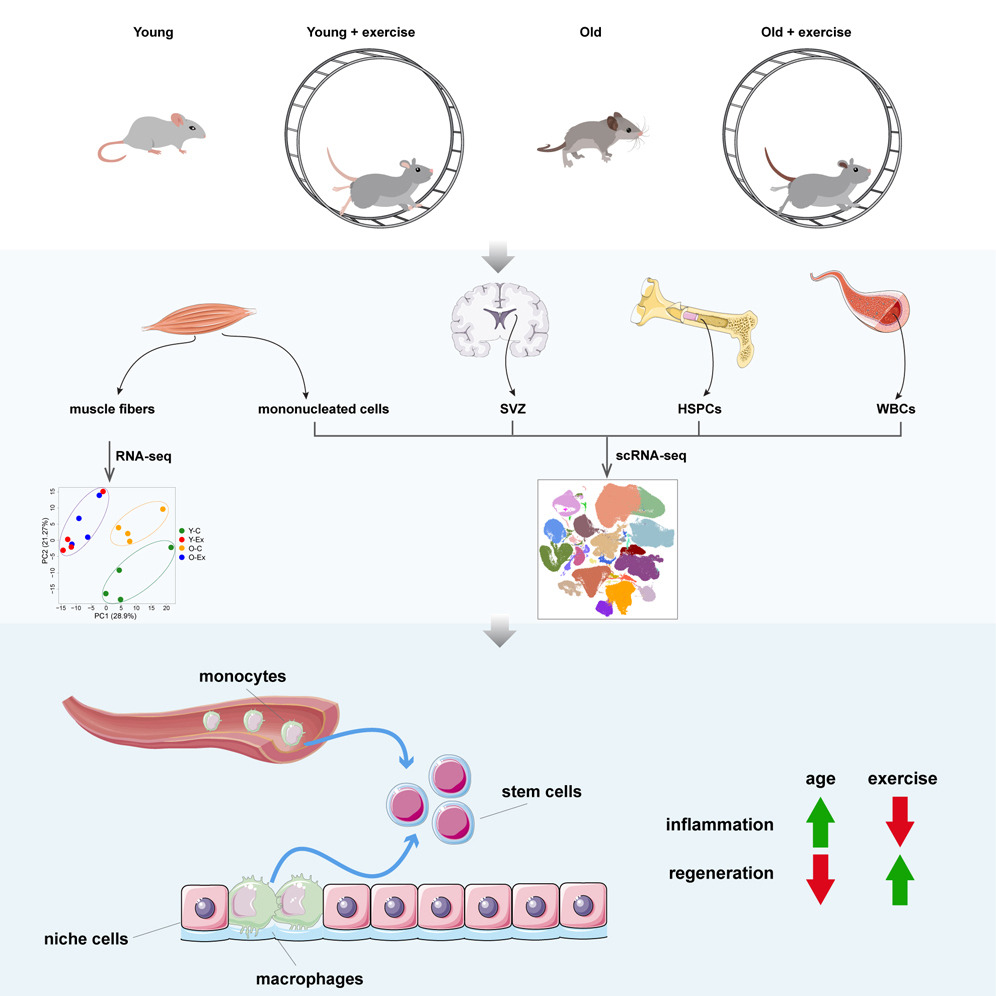
为了了解运动对干细胞及相关生态位细胞的影响,研究者选择4个月大的年轻小鼠和22个月大的年老小鼠进行了实验,小鼠们被放置到具有旋转跑轮的鼠笼中,允许它们自主使用跑轮运动5周。随后,研究者采集了小鼠骨骼肌、脑下室区(SVZ)、骨髓和血液,并对其中提取的细胞进行单细胞RNA测序,最终共选用了435628个细胞的数据。
研究者发现,随着年龄增长,激活的神经干细胞(aNSC)和成神经细胞数量减少最为显著,而运动能够使年轻小鼠和年老小鼠的这两种细胞数量增加。这与之前研究发现运动有助于成年神经发生是相符的。
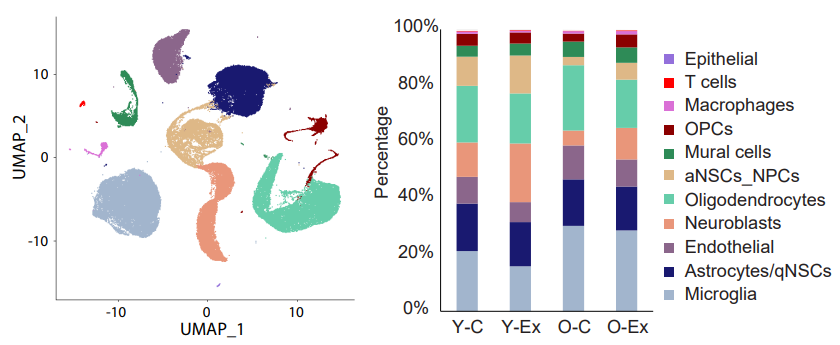
年轻小鼠(Y)、年老小鼠(O)以及运动(Ex)与否各细胞亚群的变化
在造血干细胞及相关细胞中,衰老与长期造血干细胞(LT-HSC)的增加有关,而运动会促使细胞向髓系多能祖细胞(MyMPP)扩增。
至于骨骼肌,研究者根据代谢和免疫功能相关基因表达区分了细胞亚群,这些亚群分别受到衰老和运动带来的不同影响。研究者发现,随衰老减少的亚群表现出糖酵解和线粒体呼吸的基因特征,而受运动影响的亚群表现出免疫相关的变化。
对比不同组别小鼠中细胞亚群的比例变化,研究者认为,衰老会导致细胞的变化,而运动能够一定程度上逆转这种变化。
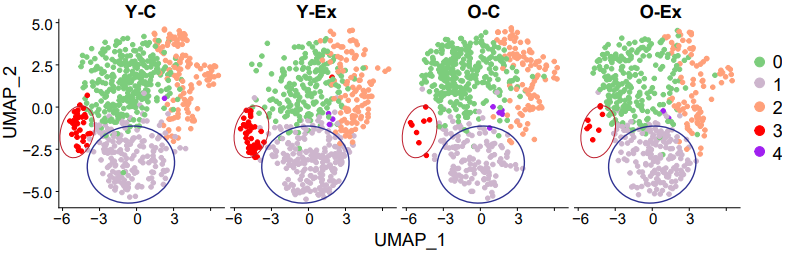
不同骨骼肌细胞亚群的变化
接下来,研究者具体分析了细胞的转录组变化。
在22种细胞类型中,研究者们发现,血单核细胞具有最多的随年龄增长表达下调的基因,达960个,而衰老肌肉的单核细胞中仅有257个。这说明来自不同组织的同一类细胞可能受衰老影响差别很大,不过它们涉及的生物学途径是相似的。
这包括各种与氧化磷酸化有关的酶亚基,以及多种与核糖体有关的基因。尤其值得注意的是,编码热休克蛋白90家族的基因受衰老影响的变化非常常见,考虑到热休克蛋白作为蛋白质折叠伴侣的作用,研究者认为这说明蛋白质组稳态的恶化可能是导致细胞衰老的通用机制。
热休克蛋白90家族基因非常常见
基因富集分析(GSEA)结果显示,虽然不同组织不同细胞类型受衰老影响表达改变的基因差异性非常大,但它们最终的落点却非常统一,清楚地显示衰老与全身炎症性环境有关,例如干扰素γ和干扰素α反应增加。
运动后,也能够在小鼠中检测到多种表达改变的基因,不过与年轻小鼠相比,在老年小鼠中改变的基因较少。但相通的是,在多种细胞中,都观察到了肿瘤坏死因子α及炎症相关通路的下调。
研究者将那些衰老影响可被运动逆转的基因称为“恢复基因”,他们发现,相较其他组织 ,肌肉中修复基因的比例更高,几乎所有肌肉细胞类型都表现出衰老过程中改变的细胞信号通路和生物过程的逆转。
另外,研究者计算了小鼠的炎症评分,发现在大多数细胞中运动都与炎症评分较低有关,但在老年小鼠中不如年轻小鼠相关性强。
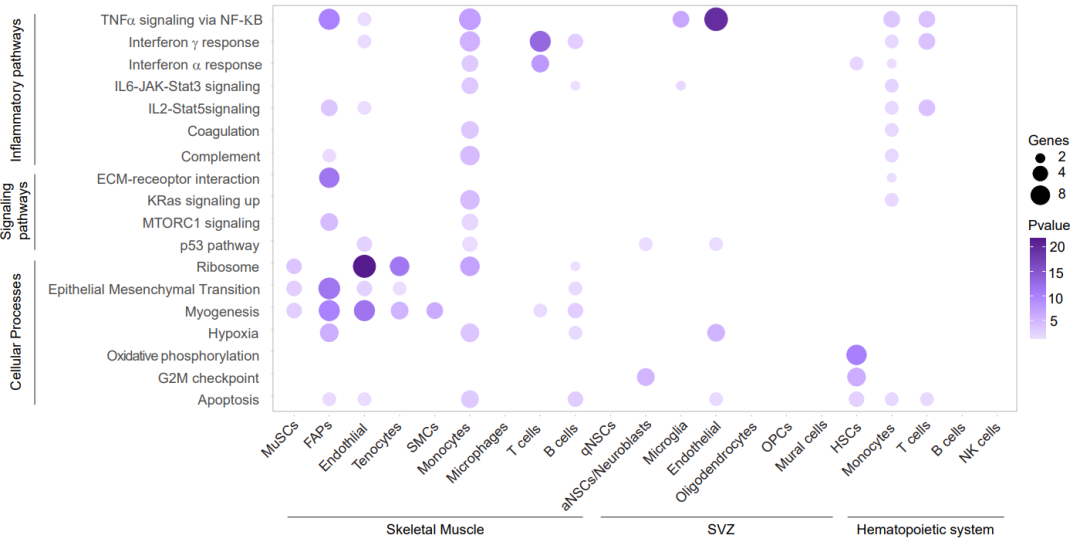
骨骼肌中恢复基因的比例更高
通过分析不同细胞亚群数量,研究者发现,衰老与出现M2巨噬细胞特征的肌肉常驻单核细胞亚群的选择性消耗有关,而运动能够增加这些细胞的数量。研究者认为,这些巨噬细胞分泌的细胞因子可能有助于运动改变局部干细胞环境。
研究者还分析了骨骼肌细胞间通讯网络,发现了38条随年龄变化的信号通路,其中一半能被运动恢复或部分恢复。
以上结果可以说明,运动能够调节骨骼肌免疫,并恢复骨骼肌干细胞生态位的胞间通讯。
类似的,研究者发现脑下室区也存在27条受衰老影响的通路,其中13条可被运动逆转。这显示运动也具有重编程神经发生区域胞间通讯来逆转大脑衰老的潜在效果。
在骨骼肌纤维中,运动降低了随衰老上调的细胞因子表达,并促进了胰岛素生长因子1、分泌型磷蛋白1、成纤维细胞生长因子2等生长因子的表达。对比运动前后的胫骨前肌, 可以发现运动显著改善了老年小鼠的肌肉再生。
由此来看,运动实在是“重现青春”的一把利器,现在的问题就是怎么克服懒惰的自己了……
参考资料:
[1]https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(23)00087-5
来自: 奇点网
更多阅读:


